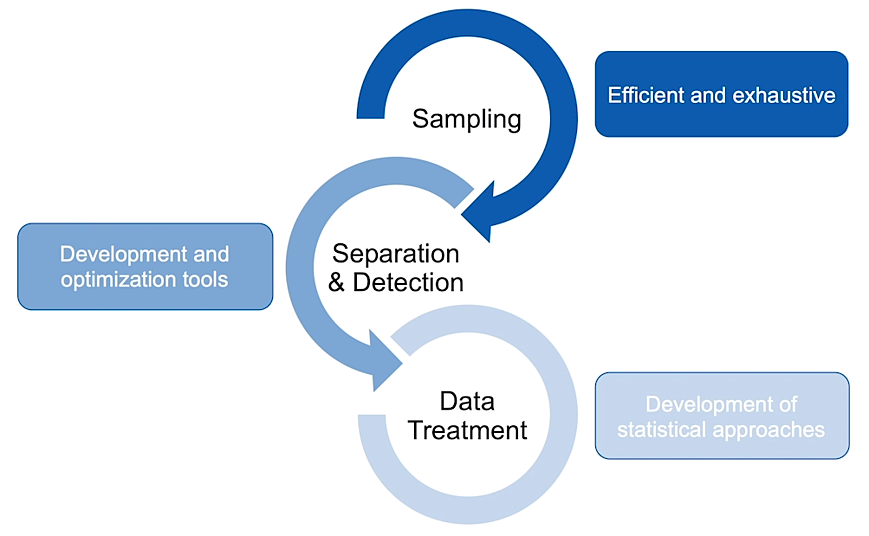
Для каждого клинического проекта групповых исследований Джеф определяет три «столпа» проекта. Прежде всего, нужно получить образцы. Затем образцы следует пропустить через масс-спектрометр для разделения и обнаружения. Наконец, полученные данные должны быть соответствующим образом обработаны, чтобы получить полезные и понятные результаты. Обработка данных некоторое время рассматривалась как самая маловажная из столпов. Однако, технологические достижения LECO развиваются так же стремительно, как и создаются новые данные, поэтому чрезвычайно важно сократить их объем и сделать их более управляемыми.
«Потому что, когда мы идем в клинику и общаемся с коллегами, им все равно, если я начну говорить: «О, период модуляции составлял 4 секунды, скорость сбора данных составляла 250 Гц…». Из вежливости они просто ответят: «Да, да», но им будет абсолютно все равно. Они просто хотят знать: это положительный образец или отрицательный образец?»
Однако, при назначении надлежащего лечения пациенту минимизация ложных отрицательных или ложных положительных результатов имеет решающее значение. Каждый из трех столпов играет решающую роль в этом процессе.
Чтобы получить результат, нужно сначала получить образец. Существует несколько способов получения образца у больного астмой, наиболее распространенными являются «инвазивные» процедуры, такие как взятие крови или сбор мокроты, бронхоальвеолярный лаваж, чистка бронхов и биопсия бронхиальной стенки. Однако, для получения образца у пациента можно также использовать забор выдыхаемого воздуха в мешки Tedlar®. Этот метод относительно быстрый и безболезненный. Пациенту легко объяснить: Вот мешок. Пожалуйста, подуйте в него.
Как только образец будет получен и доставлен в лабораторию, Pegasus® BT 4D от LEGO сможет разделить его компоненты и обнаружить сотни тысяч соединений. «В этом многие люди ошибаются», – говорит Джеф.
«Вы должны быть уверены в точности и достоверности полученных данных. Это, опять же, можно отнести к недостатку GC×GC и TOFMS, потому что инструменты настолько хороши, что в итоге вы можете иметь низкую эффективность модуляции, плохую форму пика, и все же система даст вам некоторую информацию. Однако, по-настоящему ценную информацию вы вряд ли получите. Поэтому наиболее важными являются хорошая форма пика, хорошая интенсивность пика и хорошее разделение».
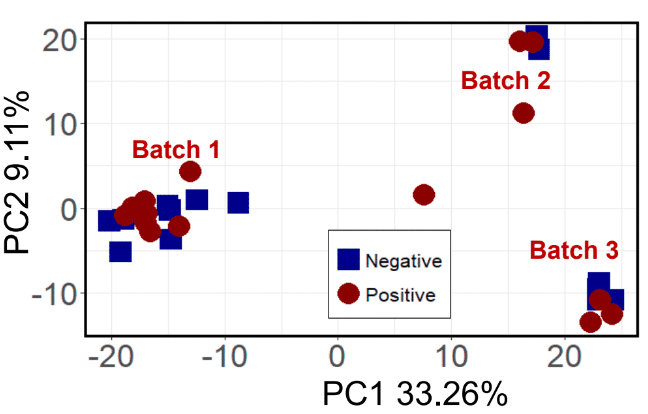
После обработки данных можно применять статистический анализ. Перед тестированием пациентов с астмой группа Джефа сначала провела несколько экспериментов с участием тестовой группы пациентов с раком легких и контрольной группы. Сначала они хотели определить, возможно ли вообще использовать образцы выдыхаемого воздуха для определения здоровья пациента. Первые обработки данных привели к некоторому разделению между группами, но в итоге они получили три отдельные группы вместо двух. Они смогли определить, что ЛОС в окружающей среде находились среди раковых ЛОС, а образцы в этих трех группах фактически были взяты в три разные время года. Хотя это было удивительно, результат ожидали получить другой.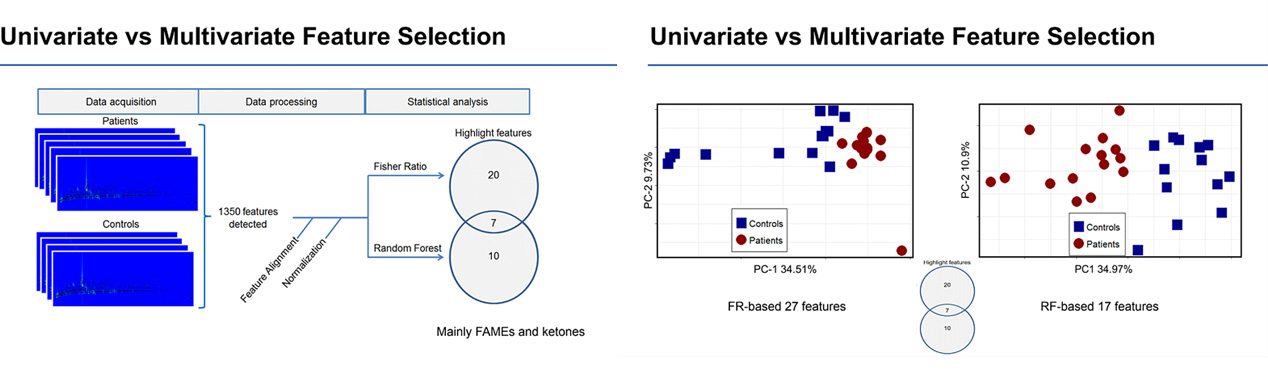
Используя различные методы классификации, Джеф смог разделить 1350 обнаруженных компонентов на два типа: 27 с коэффициентом Фишера и 17 со случайным лесом, из которых 7 перекрываются. Оттуда он смог разделить образцы на две отдельные группы: положительные на рак легких и отрицательные на рак легких.
Применяя образцы к Pegasus® GC-HRT 4D с высоким разрешением, Джеф смог глубже проанализировать составы, которые он использовал в качестве маркеров.
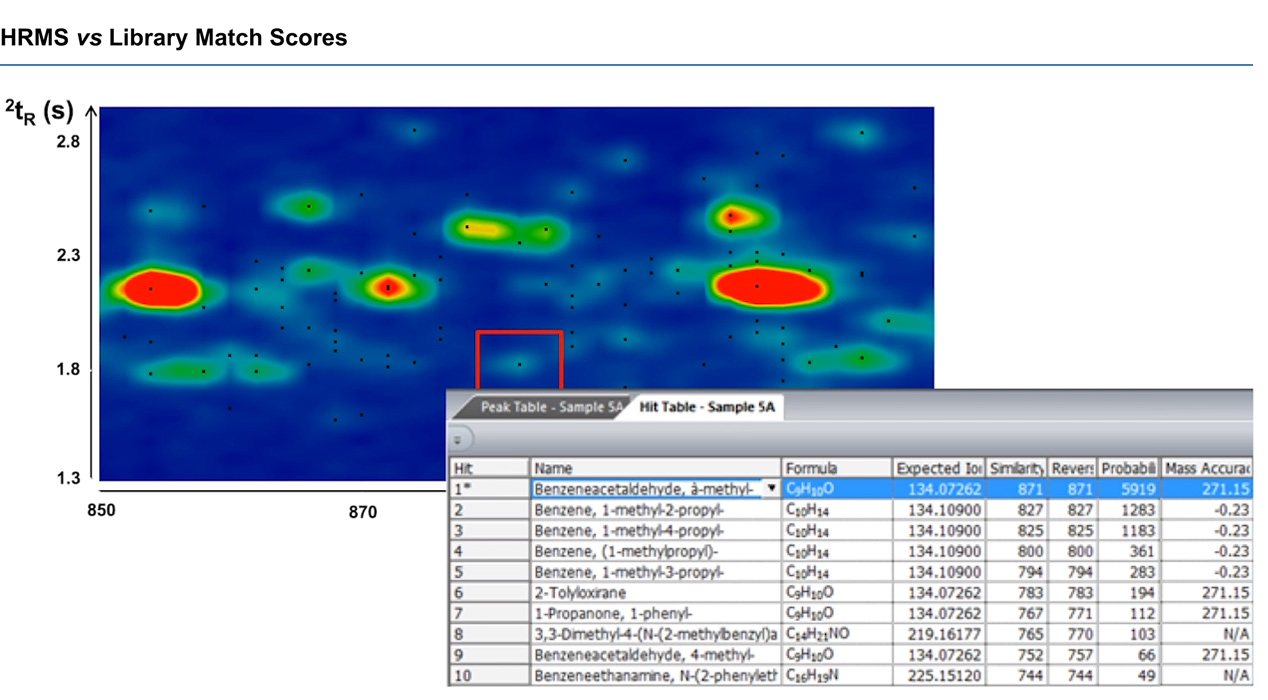
Как видно выше, отмеченный пик первоначально выглядит как бензол-ацетальдегид, с показателем совпадения в библиотеке 871. Тем не менее, масс-спектрометры с высоким разрешением позволили Джефу установить, что точность массы была слишком плохой – 271,15 м.д., тогда как следующий вероятный результат, бензол со сходством 827, имел гораздо лучшую точность массы -0,23 м.д. Используя два инструмента параллельно друг с другом, Джеф смог получить более полезную химическую информацию из имеющихся у него данных.
Проведя эти опыты, Джеф принялся за исследование астмы. За последние десять лет число случаев заболевания астмой увеличилось на 200 %. Установлено, что от этого заболевания страдают более 334 миллионов человек во всем мире, из них – 14 % детей в возрасте до 18 лет. Проблема усугубляется еще тем, что не менее 20 % пациентам с астмой назначают неправильные лекарства.
Различают два основных фенотипа астмы: нейтрофильный и эозинофильный. Нейтрофильная астма вызывается, как правило, загрязнителями и инфекциями и должна лечиться антибиотиками, а эозинофильная астма вызывается аллергенами и должна лечиться кортикостероидами. Кортикостероиды совершенно бесполезны для нейтрофильной астмы, а антибиотики неэффективны при лечении эозинофильной астмы.
Как указывалось ранее, для диагностики астмы чаще всего используются инвазивные методы, их точность составляет 67–72 %. Группа Джефа решила собрать образцы выдыхаемого воздуха у пациентов с астмой и проверить, сможет ли GC×GC-TOFMS поставить более жизнеспособный диагноз. Чтобы узнать его результаты, посмотрите полную запись утреннего семинара ASMS, проводимого в этом году, здесь.
* Этот продукт не предназначен для диагностики, лечения или профилактики каких-либо заболеваний.